Ehtimollik tushunchasi fizikada gazlarning kinetik nazariyasi rivojlanishi bilan paydo bo’ldi. Gaz juda ko’p harakatdagi zarralardan iborat ekanligi aniqlangach, gaz zarralari – uning molekulalari qanday tezliklar bilan harakatlanishi haqida savol tug’ildi.
Ingliz fizigi J. Maksvell ideal gazning birinchi nazariyasini yaratdi. Bu nazariyada gazning holati har bir zarraning holati va tezligi bilan emas, balki taqsimot funksiyasi idishning ma’lum joyida ma’lum tezlik bilan harakatlanayotgan molekulani topish ehtimoli bilan ifodalanadi. Bayon qilishni soddalashtirish uchun idish, masalan, 1 mm qirrali kubsimon yacheykalarga bo’lingan va bizni molekulaning aniq koordinatalari emas, balki uning qaysi yacheykada joylashganligi qiziqtiradi, deb faraz qilamiz. Tezliklarni ham biz aniq belgilamaymiz, balki, masalan, bu yerda OX o’q bo’ylab harakatlanuvchi molekulaning 1 mm/s dan ortiq farq qilmaydigan hamma tezligini bir xil, deb hisoblaymie. U holda tezliklarni ham o’n o’lchovli diagrammani bo’lish mumkin bo’lgan yacheykalar tarzida tasavvur qilamiz; uning o’qlari bo’yicha tezliklarning komponentlari vx, vy, vz joylashgan, nuqta esa zarraning tezligini ifodalaydi. Agar gaz molekulalariga hech qanday kuchlar, masalan, og’irlik kuchi yoki elektr maydon ta’sir etmasa, bu holda molekula idishning istagan joyida bir xil takroriylikda bo’lib turadi. Biz bunda molekulani istagan yacheykada topish ehtimolligi bir xil deymiz. Bu ehtimollikni ωi bilan belgilaymiz. Hamma yacheykalar bo’yicha olingan ωi lar yig’indisi 1 ga teng bo’lishi ravshan, chunki molekulani biror yacheykada topish ehtimoli 1 ga teng. Agar idishda N ta molekula bor bo’lsa, bitta yacheykada o’rtacha ωiN ta molekula bo’ladi, ωi ehtimollik yacheyka nomeriga bog’liq emas, i – gaz zichligi, u butun idish bo’yicha o’zgarmas.
Ma’lum tezlikdagi molekulani topish ehtimolligi yoki tezliklar diagrammasida ma’lum yacheykada nuqtani topish ehtimolligi ancha boshqacha bo’ladi. Gazning energiyasi – ye Joul aniqlangan bo’lgani uchun, qo’pol qilib aytganda, har bir molekulaga taxminan ye/N Joul to’g’ri keladi va gazda energiyasi bu kattalikdan kuchli farq qiluvchi ozgina molekulalar ham bo’lishi kerak. Tezliklar diagrammasidagi kataklar teng huquqli emas va tezliklar bo’yicha taqsimot ehtimoli bir xil emas. Ehtimolliklarning bunday taqsimotini Maksvell topdi.
Maksvell nazariyasidan, gaz molekula lari ko’p qismining tezligi 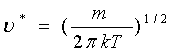 bu yerda k – Boltsman doimiysi, T –absolyut temperatura, m – molekula massasi. Bu qiymatni eng ehtimolli tezlik deyiladi. Ehtimollik tushunchasi juda ko’p foyda berdi. Uning yordamida juda ko’p zarralar ishtirok etadigan va ayrim zarralarning ahamiyati sezilarli bo’lmaydigan turli jarayonlarni hisoblab chiqish mumkin. Bular issiqlik o’tkazuvchanlik, aralashtirish – diffuziya, ximiyaviy reaktsiyalar va boshqalar. Ularni statistik fizika o’rganadi.
bu yerda k – Boltsman doimiysi, T –absolyut temperatura, m – molekula massasi. Bu qiymatni eng ehtimolli tezlik deyiladi. Ehtimollik tushunchasi juda ko’p foyda berdi. Uning yordamida juda ko’p zarralar ishtirok etadigan va ayrim zarralarning ahamiyati sezilarli bo’lmaydigan turli jarayonlarni hisoblab chiqish mumkin. Bular issiqlik o’tkazuvchanlik, aralashtirish – diffuziya, ximiyaviy reaktsiyalar va boshqalar. Ularni statistik fizika o’rganadi.
Kvant mexanika yaratilgunga qadar, ehtimolliklarning paydo bo’lishi odatda koordinatalari va tezliklarini amaliy jihatdan o’lchab bo’lmaydigan zarralarning juda katta soni bilan bog’liq deb hisoblanar edi.
Biroq, hatto, birgina ma’lum zarra uchun koordinata va impulsni bir vaqtda aniq o’lchash mumkin emas ekan va tajriba natijasini faqat ehtimollik shaklida oldindan aytish mumkin ekan. Zarra traektoriyasini aniq o’lchashning imkoni bo’lmagani uchun, demak, uchib ketayotgan proton, atom yadrosi maydonida qanday burchakka og’ishi haqidagi savolga aniq javob berish mumkin emas. Uning u yoki bu burchakka og’ishi ehtimolliginigina aytish mumkin. SHuningdek, ma’lum radioaktiv atom qachon yemirilishini ham aytib bo’lmaydi, faqat uning t sekunddan keyin yemirilish ehtimolligini ko’rsatish mumkin. Agar t = 0 da N0 ta atom bo’lgan bo’lsa, atomlar soni Nt = N0e-λt qonun bo’yicha kamayishi ma’lum. Bu formuladagi λ yemirilish doimiysi deyiladi (Radioaktivlik).
Shunday qilib, aynan qaysi atomlar yemirilishini aniqlash mumkin bo’lmasa ham juda ko’p sondagi atomlarning yemirilish qonuni to’g’risidagi da’vo to’g’ridir.
Ehtimolliklar fizikaning yana bir bo’limi–o’lchashlar nazariyasida uchraydi. Hech qaysi o’lchash o’lchanayotgan kattalikning absolyut aniq qiymatini bermaydi. Aniq qiymat o’lchangan qiymatdan farq qiladi va nazariya u yoki bu ishning faqat ehtimolligini baholashi mumkin. Takror o’lchamlar to’plamining analizidan xatolik ehtimolligini baholash–eksperimental fizikaning muhim vazifasi.
Jadvallarda, masalan yorug’lik tezligi 2,997924580(1,2)•108 m/s ga teng deb yoziladi; qavs ichidagi kattalikni standart og’ish deyiladi. Bu holda ehtimolliklar nazariyasidan yorug’likning haqiqiy tezligi yuqorida yozilgan tezligidan oxirgi raqamida 68,3% ehtimollik bilan 1,2 birlikdan ortiq farq qila olmasligi kelib chiqadi.
Gap shundaki, har qanday tajribada hisobga olinmagan ancha faktorlar bo’ladi. Yorug’lik tezligi holida temperaturaning o’zgaruvchanligi, to’lqin uzunligini o’lchashdagi noaniqlik va hokazolar shunday faktorlar bo’lishi mumkin, lekin ular verguldan keyingi sakkizinchi xonadagina seziladi. Bu tasdiqning aniqlik darajasi ehtimollik bilan baholanadi.
Ehtimolliklar nazariyasi asosiy fizik kattaliklarning aniq qiymatlarini hisoblashda juda muhimdir.