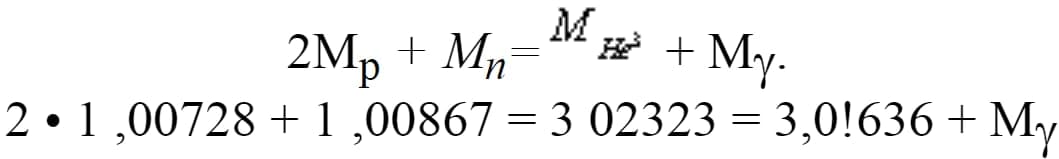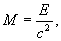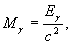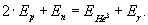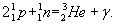M. V. Lomonosov va A.Lavuaze moddaning saqlanish qonunini massaning saqlanish qonuni sifatida ta’riflagan edilar. Ximiyaviy reaksiya qanday kechmasin, uning boshlanishida barcha tarkibiy qismlarning to’liq massasi reaksiya oxiridagi massasiga teng bo’ladi. Bundan tashqari, ximiyaviy reaksiyada unda qatnashayotgan har qanday elementlar atomlarining soni o’zgarmaydi, elementlarning atomlari faqat bir molekuladan ikkinchisiga o’tadi.
XX asrda bu qonun ancha aniqlashtirildi, chunki ko’p hollarda u noto’g’ri bo’lib chiqdi. Vodorodning geliyga aylanishi misolida bu qonunning buzilishini ko’rib chiqaylik.
Ne3 izotoplaridan birining atom yadrosi ikki proton va bir neytrondan iborat. Uning hosil bo’lish reaksiyasini kuzataylik. Bunday reaksiyami ikki bosqichda amalga oshirish mumkin. Dastlab, vodorodni neytronlar bilan nurlab, deyton - neytron va protondan iborat yadro olamiz. Bunday yadroga elektron kelib qo’shilganda vodorod atomi hosil bo’ladi, biroq uning massasi odatdagi atom massasidan ikki marta katta bo’ladi. Agar og’ir vodorodli suvni (og’ir suvni) protonlar bilan nurlansa, geliy Ne3 izotopining yadrosi hosil bo’ladi. Bunda ulkan energiya ajraladi, u γ-kvantlar, ya’ni elektromagnit to’lqinlar shaklida bo’ladi.
Bu energiya qaerdan paydo bo’ladi? Yadro zarralari - nuklonlar (neytronlar va protonlar)-yadro kuchlari bilan bir-birlariga tortiladi, yadro kuchlari faqat kichik masofalarda taxminan 1013 sm masofada ta’sir etadi, shuning uchun ana shu masofalarda ular bizga ma’lum bo’lgan boshqa kuchlardan ancha kuchli ta’sir etadi.
Neytron bilan proton birikib, deyton hosil qilishida bu zarralar tezlanadi, bunday tezlanishda har qanday zaryadli zarra elektromagnit to’lqinlarni nurlaydi.
SHunday qilib, ikkita proton va neytron bo’lgan edi, ulardan geliy yadrosi paydo bo’ldi va γ-kvantlar shaklida ulkan energiya ajralib chiqdi (Gamma-nurlanish).
Ana shu yerda massa yo’qolishi ro’y berdi. Protonning molekulyar massasi Mp=1,00728, neytron massasi Mn= 1,00867, geliy yadrosining massasi esa MHe= 3,01636. Bu yerda shunday massa birligi qabul qilinganki, unda uglerod --12S izotopining massasi 12 ga teng bo’ladi. Demak,
Agar faqat neytron, proton va geliy massaga ega, deb olinsa, u holda massaning saqlanish qonuni buziladi. Massaning saqlanish qonuni saqlanishi uchun massa gamma-nurlanishga ham xosdir, deb fikr qilish kerak. Bu yerda biz tabiat umumiy qonunining A.Eynshteyn tomonidan kashf qilingan xususiy holiga duch keldik: energiya qanday shaklda bo’lishidan kat’iy nazar jismning massasi uning energiyasi o’zgarishi bilan o’zgaradi. M massa E energiya bilan quyidagi formula orqali bog’langan:
(bu yerda s-yorug’lik tezligi), shuning uchun γ-kvantlar massasi Mγ quyidagiga teng:
bu yerda Eγ-γ-kvantlar energiyasi.
Endi massaninng saqlanish qonuni qayta tiklanmoqda, to’g’rirog’i, energiyaning saqlanish qonuni bilan birlashmoqda. Haqiqatan ham, agar tinch turgan protonga Er energiya, neytronga En energiya mos deb olsak, u holda massalarning tengligi formulasini s2 ga ko’paytirib, energiyaning saqlanish qonunini olamiz.
Reaksiyada ikki protonning elektr zaryadi Ne yadrosining zaryadiga teng ekanini (neytron - zaryadsiz zarra) sezamiz.
Bundan tashqari, chapdagi nuklonlar soni o’ngdagi nuklonlar soniga teng. Bu saqlanish qonunlariga e’tiborni jalb qilish uchun yadro reaksiyasi shunday yoziladi:
Yuqoridagi belgichalar reaksiyada ishtirok etayotgan yadro zarralarining sonini, pastdagilari esa elektron zaryadi orqali ifodalangan elektr zaryadini bildiradi. Chap va o’ngdagi yuqori belgichalar yig’indisi o’ng va chapdagi pastki belgichalar yig’indisiga teng.
Shunday qilib, massa bilan energiyaning bog’lanishi aniqlangach, massaning saqlanish qonuni energiyaning saqlanish qonuniga aylanib qoldi. Kimyoviy elemenlarning saqlanish qonuniga kelsak, bu qonun yadro reaksiyalarida amal qilmaydi (vodorod geliyga aylandi). Uning o’rniga barcha hollarda ham ikkita saqlanish qonuni: zaryadning saqlanish qonuni va nuklonlar sonining, yoki aniqrog’i, barionlar sonining saqlanish qonuni - barion zaryadining saqlanish qonuni deb ataladi - amal qiladi.